Virus viêm gan B tấn công cơ thể như thế nào?
Vùng châu Á thái bình dương có tỷ lệ và số người nhiễm HBV cao nhất của thế giới. Hơn nữa trong vùng này hầu hết các nước thuộc về thế giới đang phát triển với kinh tế còn hạn chế làm cho vấn đề chăm lo sức khỏe nói chung và bệnh nhân nhiễm HBV nói riêng có khó khăn mà Việt nam cũng không là ngoại lệ. Ở Việt nam, lây truyền HBV từ mẹ sang con và giữa các trẻ nhỏ là một nguồn lây quan trọng nên tỷ lệ trở thành mạn tính cao đồng thời bệnh có một thời gian tiến triển lâu dài trong người bệnh đủ để gây ra các biến chứng muộn và nguy hiểm như xơ gan, suy gan và ung thư gan. Một khi đã bị nhiễm HBV, do vòng đời của virus này có giai đoạn ở dạng cccDNA trong nhân tế bào giúp cho HBV tồn tại trong cơ thể hầu như suốt đời. Sự tồn tại HBV trong cơ thể ở các dạng lâm sàng khác nhau là do cân bằng động về mối tương tác giữa virus, tế bào gan và hệ thống miễn dịch của cơ thể. Nhiễm HBV từ tuổi trẻ thơ, diễn tiến tự nhiên lần lượt sẽ trải qua 3 pha là:
1) Pha dung nạp miễn dịch
2) Pha thải loại miễn dịch
3) Pha mang HBV không hoạt động.

Đặc điểm của pha dung nạp miễn dịch (pha 1) là hệ thống miễn dịch của bệnh nhân không xem HBV như kẻ lạ xâm nhập nên virus tăng sinh không bị kiềm chế. Trong pha này số lượng virus thường rất cao >2×10^6 IU/ml (>10^7 cps/ml), có HBeAg dương tính (chỉ dấu huyết thanh của virus tăng sinh) và ALT liên tục bình thường, gan không có hoặc chỉ có tổn thương tối thiểu nhưng tính lây nhiễm rất cao. Chuyển huyết thanh HBeAg tự nhiên trong pha này rất thấp gần như không xẩy ra. Khảo sát ở Việt nam, pha này thường kéo dài khoảng 20 đến 25 năm và không có chỉ định điều trị. Nhiễm HBV ở tuổi vị thành niên hay người lớn có thể không có pha này hoặc pha này chỉ xẩy ra trong một thời gian ngắn.
Đặc điểm của pha thải loại miễn dịch (pha 2) là lúc này hệ thống miễn dịch của bệnh nhân bắt đầu chống lại HBV mà biểu hiện tên lâm sàng bằng giảm lượng HBV-DNA (so với pha 1) nhưng hầu hết vẫn ở mức >10^5cps/ml, HBeAg vẫn dương tính, ALT tăng cao hoặc đôi khi có thể giao động, mô gan có tổn thương viêm và hoại tử và quá trình xơ hóa bắt đầu. Pha này kết thúc bằng việc chuyển đối huyết thanh HBeAg với xuất hiện đột biến PC (tiền lõi) hay/và BCP. Pha thải loại miễn dịch càng dài và cường độ càng cao thì tổn thương viêm hoại tử và quá trình xơ hóa gan càng nhanh và để lại nhiều hậu quả dù có chuyển sang pha mang HBV không hoạt động. Chính vì vậy mà trong pha thải loại miễn dịch nếu kéo dài thì có chỉ định điều trị đặc hiệu. Chuyển đổi huyết thanh HBeAg tự nhiên trong pha này tương đối cao vào khoảng 10% năm.
Pha mang HBV không hoạt động (pha 3) có đặc điểm là HBeAg âm tính và xuất hiện anti HBe; lượng HBV-DNA thấp từ mức không phát hiện đến <10^4 cps/ml. Về bệnh sinh, lúc này hệ thống miễn dịch đã kiểm soát được HBV. Tổn thương gan để lại do pha thải loại miễn dịch nhiều hay ít nhưng không hoặc hầu như không có tổn thương đang tiến triển thêm. Vì vậy khi chuyển sang pha mang HBV không hoạt động mà gan còn ít bị tổn thương thì tiền lượng lâu dài là tương đối tốt, biến chứng thấp. Không có chỉ định điều trị đặc hiệu trong pha này. Từ pha 3 này, bệnh cảnh lâm sàng có thể xuất hiện theo 2 hướng hoặc thuận lợi là mất HBsAg với tỷ lệ thấp từ 0,5% đến 2% mỗi năm hoặc theo hướng xấu đi tức là virus tái hoạt dưới thể viêm gan B có HBeAg âm tính hoăc quay trở về thể viêm gan B có HBeAg dương tính. Trong tình trạng tái hoạt động này có chỉ định đặc trị HBV. Chính vì các diễn biến này mà một số tác giả xem diễn tiến tự nhiên của VGV B có 4 hay 5 pha mà không nhất thiết tiếp diễn nhau.
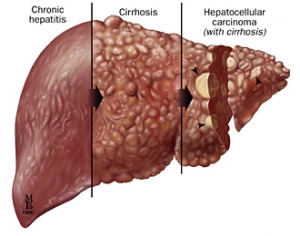
Xuất hiện xơ gan và ung thư gan trong quá trình diễn tiến tự nhiên của bệnh nhân nhiễm HBV. Tỷ lệ biến chứng xơ gan xẩy ra trên bệnh nhân nhiễm mạn tính khoảng 2% năm và và ung thư gan vào khoảng 0,5% năm. Tỷ lệ này tăng lên trên bệnh nhân có tuổi cao, nam giới, HBeAg dương tính, hay chuyển đổi huyết thanh HBeAg xẩy ra muộn sau 40 tuổi, ALT cao và đặc biệt là khi có tải lương HBV-DNA >10^4 cps/ml. Với ung thư gan thì một khi đã có xơ gan tỷ lệ biến chứng thành ung thư gan tăng cao gấp 10 lần (3% đến 6% năm) so với bệnh nhân chưa có xơ gan. Cần lưu ý là ở bệnh nhân VGV B, ung thư gan có thể xẩy ra trên bệnh nhân chưa có xơ gan với tỷ lệ đáng kể, khoảng 30%. Do đó, theo dõi phát hiện sớm ung thư gan phải thực hiện trên cả bệnh nhân chưa có xơ gan.
Typ gen HBV: Dựa vào trình tự bộ gen của HBV khác biệt nhau >8% người ta chia HBV thành các typ gen. Hiện nay đã xác định được 10 typgen của HBV là A,B,C,D,E,F,G,H,I và J. Ở Việt Nam chỉ có 2 typ gen chính là B và C (với dưới typ chính là B4 và C1). Về tính gây bệnh, HBV typ C nguy hiểm hơn typ B mà trên lâm sàng biểu hiện là: typ gen C có biến chứng xơ gan, ung thư gan cao hơn có ý nghĩa, chuyển đổi huyết thanh HBeAg chậm hơn khoảng 10 năm tỷ lệ đột biến kép BCP cao hơn và đáp ứng điều trị với IFN/P.IFN kém hơn. Đáp ứng với điều trị IFN/P.IFN thì typ gen A tốt hơn D và B tốt hơn C. Trái lại, đáp ứng điều trị giữa các typ gen HBV không khác nhau có ý nghĩa khi điều trị với thuốc uống Nucs. Vì vậy trong lâm sàng người ta không khuyến cáo phải định typ gen HBV trước khi điều trị với Nucs.

Vai trò của định lượng HBV-DNA: Ngoại trừ ở pha 1 (dung nạp miễn dịch) không có chỉ định điều trị, khi có viêm gan B hoạt động dù thể HBeAg dương tính hay âm tính có chỉ định đặc trị thì lượng HBV-DNA là một yếu tố thúc đẩy cơ bản của quá trình viêm hoại tử tại gan và trong lâu dài là biến chứng xơ gan, suy gan và ung thư gan. Bởi vậy trên lâm sàng theo dõi dựa vào định lượng HBV-DNA có một ý nghĩa tiên lượng nguy cơ rất quan trọng.
Các đột biến tự nhiên của HBV và ý nghĩa lâm sàng: HBV là một virus với cấu trúc di truyền là DNA nhưng trong vòng đời lại trải qua một giai đoạn là RNA (pgRNA) cùng với sự kiểm soát sao chép không chặt chẽ nên các đột biến tự nhiên xẩy ra cao hơn nhiều so với các virus có cấu trúc di truyền là DNA khác. Một số đột biến thường xẩy ra có tính chất làm tăng nguy cơ xơ gan và ung thư gan như các đột biến mất đoạn vùng Pre S1; Pre S2 đột biến kép vùng tiền BCP (A1762T/ G1764A) vv…. Các đột biến này cũng thường xẩy ra với typ gen C nhiều hơn với typ gen B.

Đánh giá tình trạng xơ hóa của gan: Mức độ xơ hóa của gan có ý nghĩa quan trọng trong chỉ định điều trị, theo dõi tiến triển và tiên lượng đáp ứng điều trị cũng như nguy cơ biến chứng của VGV B. Cho đến nay, sinh thiết gan vẫn được xem là tiêu chuẩn vàng để đánh giá tình trạng xơ hóa của gan dù cho còn có nhiều ý kiến phê phán. Gần đây, nhiều kỹ thuật không xâm hại được đề xuất và chấp nhận ở các mức khác nhau đã giúp giảm bớt chỉ định sinh thiết gan nhưng vẫn không thay thế hoàn toàn được sinh thiết gan. Ở Việt nam không bắt buộc sinh thiết gan trước khi điều trị VGV B và thực tế hầu như không thực hiện sinh thiết. Siêu âm đánh giá xơ gan thường kém nhạy và muộn. Một số kỹ thuật khác không xâm hại có thể sử dụng như điểm APRI, Forn, FIB-4 hay Firotest, Actitest hay Fibroscan, ARFI vv…Tuy nhiên các thầy thuốc lâm sàng phải biết đánh giá kết quả đối chiếu với những chỉ số tham khảo khác mà không máy móc dựa vào số liệu kỹ thuật đơn thuần. Điều này đòi hỏi kinh nghiệm của các bác sĩ điều trị.
