Đồng nhiễm virus viêm gan B và C
1. Giới thiệu
Tỷ lệ mắc virus viêm gan B (HBV) và virus viêm gan C (HCV) cao trên toàn cầu, liên quan với đường truyền chung của các virus này và giải thích cho những dấu hiệu thường gặp không tránh khỏi của sự đồng nhiễm HBV/HCV. Những tương tác này đã được mô tả đầu tiên khi nhiễm HCV được biết dưới dạng viêm gan không A, không B. Khó xác định một cách chính xác số lượng người bị đồng nhiễm HBV/HCV và có sự khác nhau đáng kể về mặt địa lý; ước tính 3-22% bệnh nhân nhiễm HBV mạn tính dương tính với kháng thể kháng HCV và 2-10% bệnh nhân dương tính với kháng thể kháng HCV có kháng nguyên bề mặt virus viêm gan B (HBsAg) dương tính . Bên ngoài vùng dịch lưu hành, đồng nhiễm HBV/HCV thường gặp nhất ở những nhóm riêng biệt có nguy cơ cao, đặc biệt là những người sử dụng thuốc đường tĩnh mạch, những người dương tính với virus gây suy giảm miễn dịch ở người (HIV) và những bệnh nhân đang thẩm phân máu. Các báo cáo về nhiễm HBV tiềm ẩn (HBsAg âm tính, HBV DNA dương tính) cho thấy có thể chúng ta đã đánh giá thấp tỷ lệ mắc thực của đồng nhiễm virus và ngụ ý là sự đồng nhiễm virus cần được tìm kiếm một cách tích cực bằng các xét nghiệm HBV DNA, đặc biệt là ở những người có kháng thể kháng HBc dương tính . Nhiễm 2 loại virus có thể xảy ra trong trường hợp hiếm gặp do nhiễm cấp tính đồng thời cả hai loại virus hoặc thường gặp hơn do nhiễm cấp tính virus thứ hai ở một người đã bị nhiễm mạn tính một loại virus viêm gan (bội nhiễm). Trường hợp điển hình, đặc biệt là ở những vùng có tỷ lệ mắc HBV cao, người nhiễm HBV mạn tính sẽ bị bội nhiễm HCV cấp tính. Bội nhiễm cấp tính có thể thúc đẩy viêm gan tối cấp hoặc có thể dẫn đến viêm gan mạn tính do hai loại virus với di chứng bao gồm xơ gan và ung thư biểu mô tế bào gan (HCC). Trong trường hợp hiếm gặp, bội nhiễm HCV có thể dẫn đến thanh thải HBV. Mặc dù gánh nặng bệnh tật tương đối lớn nhưng những hiểu biết liên quan đến các tương tác về virus học, hậu quả lâm sàng của đồng nhiễm và trị liệu tối ưu vẫn còn chưa đầy đủ.
2. Tương tác giữa virus trong đồng nhiễm HBV/HCV
Các nghiên cứu ở phòng thí nghiệm và trên lâm sàng đã chứng minh rằng HBV và HCV có thể tương tác với nhau và ảnh hưởng đến đáp ứng miễn dịch của vật chủ. Trường hợp điển hình, đồng nhiễm HBV/HCV liên quan với cả virus viêm gan B trong máu thấp hơn và virus viêm gan C trong máu thấp hơn so với các đối tượng nghiên cứu ở nhóm chứng nhiễm một loại virus đơn độc. Các nghiên cứu tại một thời điểm cho thấy nhiều trường hợp đồng nhiễm virus có virus viêm gan C trong máu có thể phát hiện được nhưng nồng độ HBV DNA giảm có ý nghĩa thống kê, có thể chỉ ra tính ưu thế của HCV so với HBV. Trong nhiễm virus mạn tính, sự chuyển đổi huyết thanh đối với HBsAg/kháng thể kháng HBs xảy ra với một tỷ lệ cao hơn ở những người đồng nhiễm (2,08% mỗi năm) so với những người nhiễm một loại virus đơn độc (0,43%), có thể góp phần vào sự phát triển của một dạng gọi là đồng nhiễm HBV tiềm ẩn. Điều này bất kể bằng chứng là đáp ứng tăng sinh ở tế bào bạch cầu đơn nhân máu ngoại vi phản ứng chống lại HCV nhiều hơn chống lại HBV. Sự thiếu tương đối này về sức ép miễn dịch chọn lọc trên HBV có thể dẫn đến giảm tỷ lệ đột biến ở vùng precore của HBV được quan sát thấy ở những bệnh nhân bị đồng nhiễm HBV.

Bằng chứng in vitro chỉ ra rằng protein lõi của HCV có thể tương tác trực tiếp với protein X của HBV, protein pol và RNA pregenome và nó cũng có thể ảnh hưởng gián tiếp đến Enh1 và Enh2/basal core promoter để ức chế sự phiên mã của HBV .Tuy nhiên, tính hơn hẳn của HCV so với HBV vẫn còn đang được tranh luận, với một số nghiên cứu quan sát báo cáo tác dụng ngược lại. Sự khác nhau rõ rệt có thể được giải thích bằng các phát hiện của một nghiên cứu đoàn hệ theo thời gian ở Ý trên những bệnh nhân đồng nhiễm HBV/HCV cho thấy rằng trong khi đa số HCV là dạng nhiễm virus trội, có một phổ các dữ liệu về virus học phức tạp hơn với dấu hiệu mối quan hệ về động học và tính đồng trội biến đổi xảy ra đến 1/3 bệnh nhân (Hình 1).
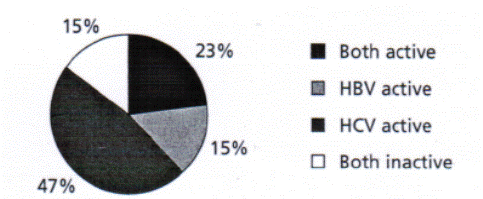
Hình 1 Mô hình hoạt động của virus trong số các bệnh nhân đồng nhiễm HBV/HCV (N=103). (Dựa trên các dữ liệu từ Raimondo và cộng sự )
3. Sự tiến triển đến xơ hóa và ung thư biểu mô tế bào gan (HCC) trong đồng nhiễm HBV/HCV
Các nghiên cứu tại một thời điểm báo cáo là những bệnh nhân có HBsAg dương tính kèm nhiễm HCV hoạt động cho thấy xơ gan nặng hơn và tiến triển đến xơ gan nhanh hơn so với những bệnh nhân chỉ nhiễm một loại HCV. Một nghiên cứu đa trung tâm ở Ý trên 59 bệnh nhân đồng nhiễm virus đã chứng minh rằng nhiễm HBV và HCV cùng tồn tại có liên quan với tỷ lệ mắc xơ gan cao hơn nhiễm một loại HBV đơn độc (28,8% so với 15,1%)
Các dữ liệu dịch tể học từ một phân tích tổng hợp lớn cho thấy là có thể có một tác dụng hiệp đồng gây ung thư giữa hai loại virus, với một tỷ số chênh đối với ung thư biểu mô tế bào gan (HCC) là 35,7 (26,2-48,5,khoảng tin cậy (CI) 95%) ở những người đồng nhiễm virus hoạt động so với 14,1% (10,6-18,8, khoảng tin cậy 95%) ở những người nhiễm HBV đơn độc và 4,6% (3,6-5,9, khoảng tin cậy 95%) ở những người nhiễm HCV đơn độc .Ngay cả khi HBV không hoạt động (HBsAg âm tính, kháng thể kháng HBc dương tính) và rõ ràng không góp phần vào phản ứng viêm, vẫn tăng nguy cơ phát triển ung thư biểu mô tế bào gan gấp 2-2,5 lần.
4. Điều trị đồng nhiễm HBV/HCV
Các hướng dẫn được thiết lập để điều trị những bệnh nhân đồng nhiễm HBV/HCV đã bị trở ngại do thiếu chứng cứ có chất lượng cao về hiệu quả điều trị vì đồng nhiễm là một tiêu chuẩn loại trừ trong đa số thử nghiệm lâm sàng lớn. Ngoài ra, nhiều bệnh nhân bị đồng nhiễm HBV/HCV ở các nước phương Tây không phù hợp với các thử nghiệm lâm sàng, do sự nhiêm HIV thêm hoặc do lối sống hỗn loạn liên quan với việc sử dụng thuốc tiêm ở một số bệnh nhân mắc viêm gan gần đây. Dựa vào phần lớn chứng cứ về tính trội hơn của nhiễm HCV so với nhiễm HBV, các hướng dẫn của châu Âu mới đây gợi ý rằng điều trị khởi đầu nên nhắm đích là HCV . Khi HCV được làm sạch, có nguy cơ tái hoạt HBV tiềm ẩn mà sau đó có thể cần phải điều trị bằng các chất tương tự nucleos(t)ide.
Hai thử nghiệm ngẫu nhiên kiểm tra hiệu quả của việc điều trị chuẩn HCV (peginterferon alfa-2a/2b và ribavirin) trong đồng nhiễm HBV/HCV. Những bệnh nhân bị nhiễm HCV (alanine aminotransferase huyết thanh > 1,5 lần giới hạn trên của mức bình thường, RNA > 105 bản sao (copies)/mL), có HBsAg có thể phát hiện được (N=161) hoặc không có HBsAg có thể phát hiện được (N=160) đã được nghiên cứu ở Taiwan. Các bệnh nhân nhận được điều trị chuẩn trong 24/48 tuần theo genotype với peginterferon alfa 180 mg/tuần cộng ribavirin 800-1200 mg/ngày. Theo dõi 6 tháng sau khi hoàn tất điều trị cho thấy tỷ lệ đáp ứng virus kéo dài (SVR) không khác nhau giữa những người đồng nhiễm virus so với người chỉ nhiễm HCV đơn độc: 72,2% ở bệnh nhân đồng nhiễm virus genotype 1 so với 77,3% bệnh nhân nhiễm một loại virus đơn độc genotype 1, và 82,8% so với 84% ở những bệnh nhân genotype 2 và 3. Trong số bệnh nhân có HBV DNA trên 1000 IU/mL lúc bắt đầu điều trị, 45% bệnh nhân đã đạt được đáp ứng virus đối với HBV vào lúc 24 tuần; 19 bệnh nhân trước đây có HBV DNA không phát hiện được đã tăng tải lượng HBV DNA.
Một thử nghiệm nhỏ hơn đa trung tâm theo thời gian HELP-NET ở châu Âu về peginterferon alfa-2b và ribavirin bao gồm 19 bệnh nhân (10 genotype 1, 9genotype 2/3) đã được công bố đầy đủ. Tổng số 15 bệnh nhân đã hoàn tất việc điều trị và theo dõi sau điều trị trong 24 tuần. Vào lúc 24 tuần sau khi điều trị, tỷ lệ đáp ứng virus kéo dài (SVR) đã quan sát thấy ở86% bệnh nhân genotype 1 và 100% bệnh nhân genotype 2/3. 2 trong số 6 bệnh nhân là những người đầu tiên có HBV DNA phát hiện được đã sạch loại HBV có thể phát hiện được và 4 bệnh nhân có tải lượng HBV có thể phát hiện được lúc ban đầu đã có của HBV. Tần suất các phản ứng phụ nghiêm trọng phù hợp với các thử nghiệm nhiễm một loại virus đơn độc trước đây.
Cả hai nghiên cứu đã chứng minh là các đề cương điều trị chuẩn HCV có thể áp dụng đối với những người đồng nhiễm HBV/HCV; tuy nhiên nên theo dõi sát tải lượng virus HBV, ngay cả khi bệnh nhân có HBV DNA không thể phát hiện được lúc bắt đầu điều trị. Kết luận tương tự đã được đưa ra sau khi điều trị với interferon không pegylate hóa và ribavirin ở 42 bệnh nhân đồng nhiễm virus trong một nghiên cứu của Chuang và cộng sự. Chỉ có 1 trong số 42 bệnh nhân đã sạch đồng thời HCV và HBV khi dùng interferon và ribavirin, mặc dù 5 bệnh nhân (11,9%) xuất hiện sự chuyển đổi huyết thanh HBsAg trong thời gian theo dõi (đến 72 tuần). Thanh thải HBV tương quan nghịch biến với đáp ứng virus kéo dài (SVR) đối với HCV. Potthoff và cộng sự đã báo cáo một trường hợp đồng nhiễm HBV/HCV được điều trị bằng peginterferon và ribavirin trong đó sự phối hợp liệu pháp kháng virus và gây miễn dịch chủ động đối với HBV đã đạt được sự thanh thải thành công cả hai loại virus với sự phát triển kháng thể kháng HBs chuẩn độ cao.
Không có nghiên cứu nào trong số này kiểm tra về vai trò của nucleos(t)ide trong điều trị đồng nhiễm virus. Các dữ liệu ở lãnh vực này đặc biệt còn hạn chế, giới hạn trong một nghiên cứu đơn trên 8 bệnh nhân được cho dùng interferon chuẩn cộng lamivudine; đáp ứng virus kéo dài đối với HCV đã đạt được ở 50% bệnh nhân và thanh thải HBeAg đã được quan sát thấy ở 3 bệnh nhân . Không có nghiên cứu nào kiểm tra việc sử dụng các nucleos(t)ide mạnh hơn trong trường hợp đồng nhiễm virus.
5. Tóm tắt
Đồng nhiễm virus viêm gan B (HBV)/virus viêm gan C (HCV) là một tình trạng thường gặp nhưng chưa được nghiên cứu đầy đủ, đặc biệt ở những vùng dịch lưu hành. Tương tác xảy ra giữa 2 loại virus cả về mức độ virus học và quan trọng hơn là mức độ gây bệnh ở đó đồng nhiễm virus thúc đẩy bệnh tiến triển nhanh và tăng nguy cơ bị ung thư biểu mô tế bào gan. Đáp ứng điều trị HCV với peginterferon và ribavirin dường như tương tự giữa đồng nhiễm virus và nhiễm một loại virus đơn độc, tuy nhiên khả năng tái hoạt hồi ứng của HBV khi điều trị ức chế bắt buộc phải có sự giám sát. Các nghiên cứu kiểm tra việc sử dụng liệu pháp phối hợp với interferon,ribavirin và các nucleos(t)ide mạnh là vấn đề cấp thiết.
